Que faut-il savoir sur les detergents?
Detergents ALcaLInS, neutres et acides

Le nettoyage des équipements de production d'aliments ne peut être efficace que lorsque les quatre axes du célèbre ‘cercle de Sinner’ sont présents: énergie thermique (température), activité chimique (détergents), action mécanique (écoulement manuel, gravitationnel ou turbulent) et temps de contact (temps de nettoyage). Les détergents modifient les propriétés physico-chimiques de l'eau afin que le liquide de nettoyage puisse mieux pénétrer la saleté, la détacher et l'entraîner. Pour un nettoyage efficace, il convient donc de choisir le bon produit. Découvrez ici nos conseils!
Les Etapes du nettoyage
Le nettoyage se déroule en trois étapes: détacher la saleté organique et inorganique de la surface par des processus physiques et chimiques, disperser la saleté dans la solution de nettoyage, et enfin l'empêcher de se déposer à nouveau sur la surface. La formulation du détergent doit contenir tous les composants nécessaires à ces différentes étapes.
Rôle des agents chimiques
La première étape nécessite des composants chimiques qui réduisent la tension de surface et permettent ainsi de mieux mouiller la surface. Ils doivent également permettre au liquide de nettoyage de pénétrer dans la saleté et les pores de la surface du substrat à nettoyer. La saleté se dissout plus facilement à l'aide de composants chimiques qui dispersent et séquencent la saleté organique et inorganique respectivement.
La deuxième étape nécessite des agents chimiques ayant d'excellentes propriétés de suspension et d'émulsification. Ils doivent donc être capables de maintenir en suspension les particules de saleté insolubles et d'émulsionner ou de disperser l'huile et la graisse.
Dans la troisième étape, le pouvoir de dispersion et de séquençage des mêmes ingrédients actifs est à nouveau mis à contribution, comme l'exigeaient les étapes 1 et 2.
Il existe des formulations de détergents à plusieurs composants, disponibles en types alcalin, neutre ou acide.
La bonne formulation a chaque etape
Il n'existe pas de nettoyant universel pour l'élimination de tous les types de salissures sur n'importe quelle surface. Pour chaque dispositif ou type de sol, une analyse doit être effectuée pour déterminer quelle formulation permettra d'atteindre la pureté requise sans endommager la surface du matériau.
Conseils des fabricants
En général, ce sont les fabricants de détergents qui vous proposeront une solution adaptée à vos besoins. Toutefois, la sécurité alimentaire reste la responsabilité finale du fabricant de denrées alimentaires. Ce dernier est donc également responsable de la pureté de ses équipements de production et de l'environnement dans lequel il opère. Il ne peut donc pas simplement accepter une formulation sans effectuer lui-même une évaluation approfondie et vérifier les recommandations du fournisseur de détergent par rapport à la pratique.
Critères de choix
Le choix du détergent dépend avant tout du type de saleté à éliminer et surtout du niveau de pureté à obtenir (pureté physique, chimique ou microbiologique). D'autres considérations sont également prises en compte, telles que la dureté de l'eau de nettoyage utilisée, la vitesse à laquelle le détergent peut être rincé, l'exigence en matière de résidus de détergent sur la surface, le coût, la sécurité d'utilisation, les risques pour l'utilisateur et l'environnement, les exigences légales, etc.
formulations alcalines
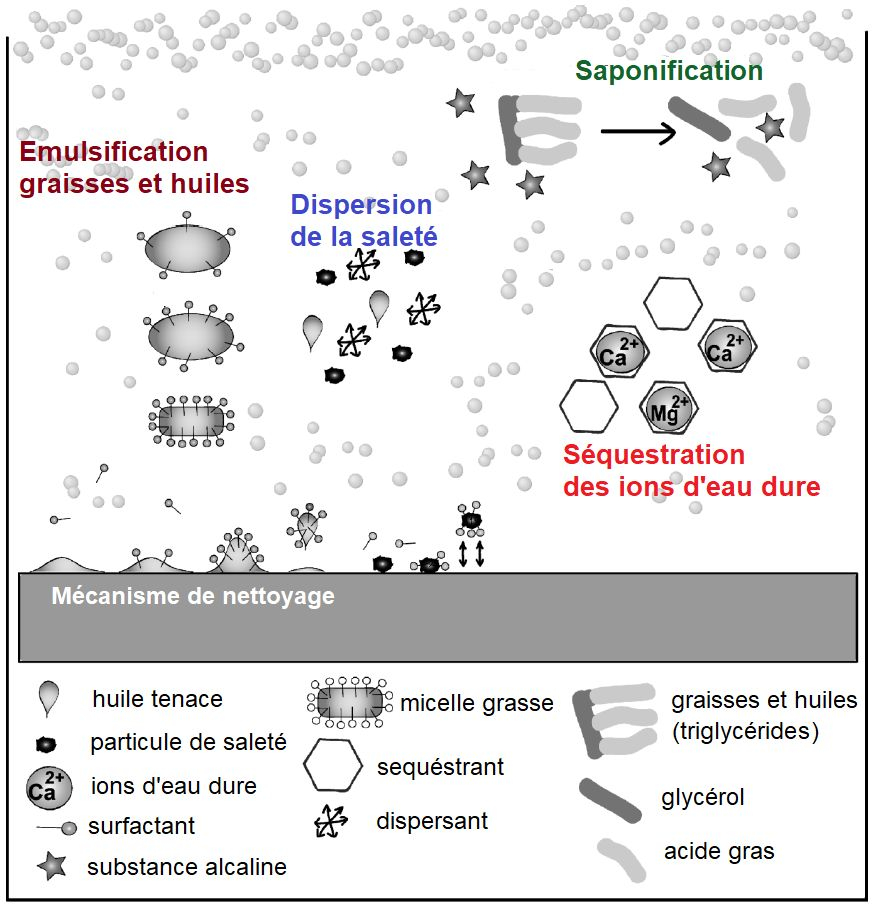
Les formulations de détergents alcalins sont utilisées pour éliminer les résidus organiques. Le principal composant est le NaOH ou le KOH, qui sont tout aussi puissants pour l'hydrolyse (saponification) et la peptification des graisses et des protéines, respectivement. Bien qu'une solution de nettoyage à base de KOH soit plus facile à évacuer, son utilisation est plutôt limitée à l'industrie pharmaceutique en raison de son prix plus élevé.
Tensioactifs
Les agents de surface ont différentes fonctions: mouillage, pénétration de la saleté, suspension, dispersion et émulsification. En abaissant la tension superficielle de l'eau, il est possible de mieux mouiller la surface à nettoyer. La saleté s'enlève alors plus facilement. Les détergents utilisent le plus souvent agents de surface non ioniques, parfois en combinaison avec des agents de surface amphotères qui créent un effet ‘microbiocide’. Les tensioactifs anioniques ont un effet moussant trop fort, ce qui complique le rinçage. Enfin, les agents de surface cationiques sont les moins efficaces, mais ils ont l'effet microbicide le plus élevé.
Agents tampons, séquestrants et inhibiteurs de corrosion acide
Les silicates, polyphosphates, borates et citrates appartiennent à la catégorie des 'agents tampons' car ils augmentent l'efficacité de ces agents de surface et peuvent mieux maintenir en suspension les résidus éliminés. Les séquestrants stochiométriques, tels que l'EDTA, le NTA et les gluconates, sont actifs comme complexants dans des rapports stochiométriques stricts, dans le but de contrer la dureté de l'eau de nettoyage et d'améliorer l'élimination des constituants inorganiques. Les agents séquestrants tels que les phosphonates, les polyphonates et les polyacrylates, sont actifs dans des proportions sous-stoechiométriques, empêchant la formation de calcaire lors du rinçage des équipements nettoyés à l'eau dure. L'EDTA et le NTA n'ont pas ce potentiel car ils sont trop dilués en ions complexes Ca- et Mg-.

Effet moussant
En outre, des agents de surface non ioniques hydrophobes sont ajoutés pour limiter l'effet moussant. Un moussage excessif rend le nettoyage moins efficace et demande plus de temps de rinçage. Néanmoins, certains produits de nettoyage fonctionnent sur le principe que les mousses adhésives ont le temps de pénétrer et de détacher la saleté, puis de la faire graviter vers le sol de l'usine et le réseau d'égouts. Ce type de mousse peut ensuite être facilement éliminé par rinçage.
Formulations neutres

On privilégie des formulations de détergents neutres lorsque la surface du matériau à nettoyer risque d'être endommagée par le NaOH et le KOH (p.ex., l'aluminium, les surfaces métalliques galvanisées ou d'autres matériaux sensibles). On tente de réduire le pH à 6-8 en remplaçant les composants alcalins classiques (NaOH ou KOH) par des substances neutres telles que des silicates, des phosphates, des phosphonates et des citrates. Ils rendent la solution de nettoyage légèrement alcaline et assurent l'effet tampon nécessaire. Comparés au NaOH et au KOH, ils ont un effet mouillant plus fort, sont plus efficaces pour déplacer la saleté et ont aussi un meilleur effet dispersant et émulsifiant. Ils sont non corrosifs et ne laissent pas ces dépôts blancs de Na2CO3 et K2CO3 que l'on voit souvent lors de l'utilisation de NaOH et de KOH. L'inconvénient est qu'ils sont plus chers.
Les tensioactifs sont aussi présents ici, avec à nouveau la préférence pour les agents de surface non ioniques. Des enzymes telles que les protéases et les lipases peuvent aussi être présentes dans le détergent. Elles éliminent les couches de protéines et de graisses plus récalcitrantes en l'absence de tensioactifs. Comme elles sont moins agressives que les détergents ‘classiques’, les formules à base d'enzymes sont souvent utilisées pour le nettoyage des installations de filtres à membrane. Elles sont également utilisées pour le nettoyage des échangeurs de chaleur à plaques et à tubes.
Formulations acides
Les dépôts minéraux sur les équipements sont pratiquement impossibles à éliminer avec des agents de nettoyage alcalins. En fait, les substances alcalines contribuent même d'une certaine façon à la formation de ces dépôts. Seul un cycle de nettoyage acide peut dissoudre et éliminer ces dépôts de sel inorganique et de calcaire. Les formulations de détergents acides peuvent être utilisées pour produire des solutions ayant un pH de 2,5 ou moins. Il s'agit généralement de ‘mélanges’ d'acides inorganiques et organiques, et de sels agissant comme des acides (p.ex. des composés d'ammonium).
Acides inorganiques

Les acides inorganiques, tels que l'acide nitrique (HNO3), l'acide sulfurique (H2SO4) et l'acide phosphorique (H3PO4), produisent des solutions de nettoyage fortement acides qui présentent l'inconvénient d'être corrosives et de précipiter certains sels solubles. De plus, leur utilisation n'est pas sans risque en termes de sécurité (irritation de la peau, des yeux, etc.) et ils peuvent également abîmer les vêtements des opérateurs de nettoyage.
Les solutions à base d’acide nitrique pour une concentration de 1 à 2% permettent d'éliminer le calcaire, les pierres de lait, le tartre, etc. Elles sont utilisées pour nettoyer et déminéraliser les échangeurs de chaleur. Les vapeurs d'azote peuvent rendre le travail des opérateurs plus difficile et représentent un risque pour leur peau et leurs yeux. En raison du pouvoir oxydant de l'acide nitrique, il ne peut pas être utilisé en combinaison avec des agents de surface. Lorsque cet acide est utilisé, les nitrates sont renvoyés dans l'installation de traitement des eaux, puis rejetés dans les eaux de surface. Ils peuvent entraîner une eutrophisation: croissance excessive des algues due à un excès de nutriments, entraînant un manque d'oxygène et la mortalité des poissons. Les gouvernements imposent donc une charge sur les rejets excessifs de nitrates dans les eaux de surface.
L’acide sulfurique est corrosif pour l'acier inoxydable, et doit donc être formulé avec un inhibiteur de corrosion. L'H2SO4 en solution à 1% est le détergent acide le moins cher, mais il n'est pas vraiment rentable en raison de son pouvoir nettoyant plutôt modéré et de son utilisation limitée jusqu'à 40 °C. Néanmoins, il est utilisé dans des solutions de désinfection où un pH faible est nécessaire pour obtenir une activité biocide optimale. Le H2SO4 pose également d'autres problèmes. Les sels de sulfate contribuent à une charge saline plus élevée dans l'effluent et, dans des conditions aérobies, ils peuvent endommager les murs en béton des stations d'épuration des eaux usées. En conditions anaérobies, du H2S peut se former, même à de faibles concentrations de sulfates. L'utilisation d'acides phosphoriques et organiques est donc plus courante et plus appropriée.
L’acide phosphorique offre la solution idéale, car il est moins corrosif et est également utilisé comme acide alimentaire. Les phosphates contribuent naturellement à une plus grande charge en sel dans les eaux usées, et ont eux aussi l'inconvénient supplémentaire de contribuer à l'eutrophisation des eaux de surface. C'est pourquoi les gouvernements prélèvent également des taxes sur les rejets excessifs de phosphates dans ces eaux. Mais comme la plupart des entreprises alimentaires ne disposent pas d'une station d'épuration des eaux usées avec élimination des phosphates, elles sont obligées de préférer les acides organiques à l'acide phosphorique.
Les acides organiques sont presents naturellement ou utilises comme additif (numero E) dans certains aliments
Acides organiques
Les acides organiques typiques sont l'acide formique, l'acide acétique, l'acide citrique, l'acide tartrique, l'acide lactique et l'acide gluconique. Ils présentent plusieurs avantages. Tout d'abord, ce sont des acides alimentaires, car ils sont présents naturellement ou utilisés comme additif (avec le numéro E) dans certains aliments. De plus, ils sont moins agressifs et moins dangereux à l'emploi que les acides inorganiques, et ils sont moins corrosifs. Bien qu'ils soient plus facilement biodégradables, ils peuvent entraver la dégradation de grandes quantités de matières organiques difficiles à dégrader dans les eaux usées. En effet, ils contribuent également à une charge de DCO/BOD plus élevée dans le traitement de l'eau. Ces problèmes surviennent principalement dans les stations d'épuration des eaux usées dont la capacité de traitement est insuffisante, c'est-à-dire dont l'apport en oxygène est insuffisant comme facteur limitant.
L'acide peracétique est actif à la fois comme détergent et comme désinfectant dans des conditions acides, et ne mousse pas. Son odeur est assez désagréable, et il peut provoquer de la corrosion et également attaquer les joints en caoutchouc. Des valeurs trop élevées d'acide peracétique dans le traitement des eaux usées sont également désastreuses pour la biomasse, ce qui rend le traitement des effluents plus complexe.
L’acide sulfamique, un solide hydrosoluble, est souvent utilisé pour éliminer la rouille ou le calcaire. Il est moins volatile et toxique que les acides inorganiques; mais bien que moins corrosifs, les inhibiteurs de corrosion sont toujours nécessaires.
Les acides sulfoniques sont des acides plus forts que les acides organiques et sont donc souvent utilisés comme alternative. Ils se dissolvent très bien dans l'eau, sont non oxydants et ont le pouvoir détergent nécessaire.
En plus des acides, des agents de surface non ioniques et anioniques peuvent à nouveau être présents pour éliminer les salissures organiques résiduelles, les résidus de graisse et les dépôts minéraux. Des tensioactifs hydrophobes non ioniques sont à nouveau ajoutés comme agents antimousse, ainsi que des acides phosphoniques pour limiter la corrosion de l'inox.Activité des formulations alcalines
